
Gaz Halindeki Maddeler
Gaz halindeki maddeler, belirli bir şekil veya hacim taşımadan bulundukları ortamı dolduran düşük yoğunluklu fazlardır. Bu yazıda gazların fiziksel özellikleri, davranış kanunları ve çeşitli uygulama alanları ele alınmaktadır. Gazların bilimsel ve endüstriyel anlamdaki önemi vurgulanmaktadır.
| Gaz halindeki maddeler, maddenin üç temel hali olan katı, sıvı ve gaz arasında yer alan bir fazdır. Gazlar, belirli bir şekil veya hacim taşımayan, çevrelerindeki ortamın hacmini dolduran ve genellikle düşük yoğunluklu olan maddelerdir. Bu makalede, gaz halindeki maddelerin fiziksel özellikleri, davranışları ve uygulama alanları ele alınacaktır. Gazların Fiziksel Özellikleri Gazların bazı temel fiziksel özellikleri şunlardır:
Gazların Davranış Kanunları Gazların davranışlarını açıklamak amacıyla geliştirilen birkaç temel yasa bulunmaktadır:
Gaz Halindeki Maddelerin Uygulama Alanları Gaz halindeki maddeler, birçok alanda önemli uygulamalara sahiptir:
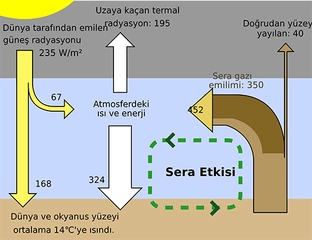
Sonuç Gaz halindeki maddeler, fiziksel özellikleri ve davranışları açısından benzersizdir. Bu özellikler, gazların çeşitli endüstrilerde ve bilimsel çalışmalarda geniş bir uygulama yelpazesine sahip olmasını sağlar. Gazların davranışlarını anlamak, hem teorik hem de pratik açıdan önemlidir. Bu nedenle, gazlarla ilgili çalışmalar ve araştırmalar, kimya ve fizikteki temel konular arasında yer almaktadır. Ekstra Bilgiler Gaz halindeki maddelerin özelliklerinin yanı sıra, gazların çevresel etkileri de dikkate alınmalıdır. Özellikle sera gazları, iklim değişikliği ile ilgili önemli bir faktördür. Karbondioksit, metan ve diğer sera gazlarının atmosfere salınması, dünya iklimini etkileyen önemli bir sorundur. Gazların kontrolü ve yönetimi, sürdürülebilir bir geleceğin sağlanması açısından kritik öneme sahiptir. Bu makale, gaz halindeki maddelerin temel özellikleri, davranışları ve uygulama alanları hakkında kapsamlı bir bakış sunmayı amaçlamaktadır. Gazların bilimsel ve endüstriyel öneminin yanı sıra, çevresel etkileri üzerinde de durulmuştur. |







































Gaz halindeki maddeler arasında doğada bulunan gazların özellikleri ve davranışları üzerine düşündüğümüzde, hangi gazların en yaygın olduğunu merak ediyorum. Örneğin, azot ve oksijen dışında hangi gazların doğal süreçlerde önemli rol oynadığını biliyor musunuz? Gaz olan maddelerin çevremizdeki etkileri neler?
Gazların Yaygınlığı ve Önemi
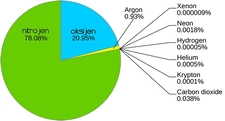
Gaz halindeki maddeler arasında en yaygın olanları elbette azot ve oksijendir. Bununla birlikte, doğada bulunan diğer önemli gazlar arasında karbondioksit, metan ve argon da bulunmaktadır. Karbon döngüsü içerisinde karbondioksit, bitkilerin fotosentez yapabilmesi için kritik bir öneme sahiptir. Metan ise, özellikle sera gazları arasında önemli bir yer tutar ve iklim değişikliği üzerinde büyük bir etkiye sahiptir.
Doğal Süreçlerde Gazların Rolü
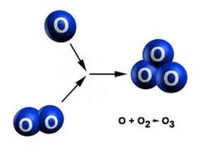
Başka bir önemli gaz olan su buharı, iklim ve hava koşullarının oluşumunda rol oynar. Su buharı, atmosferdeki sıcaklık dengesini sağlamada kritik bir faktördür. Ayrıca, ozon gazı da atmosferin üst katmanlarında bulunarak, güneşin zararlı UV ışınlarını süzmekte önemli bir görev üstlenmektedir.
Gazların Çevre Üzerindeki Etkileri
Gazların çevremizdeki etkileri oldukça çeşitlidir. Örneğin, insan faaliyetleri sonucu salınan sera gazları iklim değişikliğine neden olurken, hava kalitesinin bozulmasına da yol açmaktadır. Özellikle endüstriyel atıklar ve araç egzozlarıyla salınan gazlar, hava kirliliğine ve buna bağlı sağlık sorunlarına neden olmaktadır. Ayrıca, doğal gaz gibi enerji kaynakları da çevresel etkileri bakımından dikkatle yönetilmesi gereken maddelerdir.
Sonuç olarak, doğada bulunan gazların çeşitliliği ve bunların çevremizdeki etkileri, hem ekosistem dengesi hem de insan sağlığı açısından önemli bir konudur.
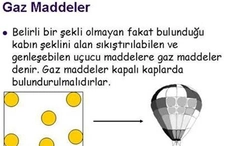
Gaz halindeki maddelerin belirli bir hacmi veya şekli olmadığından bahsediliyordu. Peki, bu durum gazların neden her oranda karışabildiğini ve homojen karışımlar oluşturduğunu nasıl açıklar? Gazların sıcaklık ve basınç değişikliklerine karşı bu kadar hassas olmasının sebebi nedir?
Merhaba Tabnak,
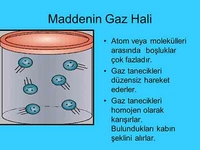
Gazların belirli bir hacimleri veya şekilleri olmadığı için bulunduğu kabın hacmini ve şeklini alırlar. Bu nedenle gaz molekülleri arasındaki etkileşim neredeyse yok denecek kadar azdır ve bu moleküller serbest bir şekilde hareket edebilirler. Bu serbest hareket, gaz moleküllerinin birbirleriyle kolayca karışmasını ve homojen karışımlar oluşturmasını sağlar.
Sıcaklık ve Basınç Değişikliklerine Hassasiyet: Gaz molekülleri arasındaki zayıf etkileşimler, gazların sıcaklık ve basınç değişikliklerine karşı daha duyarlı olmasına neden olur. Sıcaklık arttığında, gaz moleküllerinin kinetik enerjisi artar ve moleküller daha hızlı hareket ederler, bu da gazın genleşmesine neden olur. Basıncın artmasıyla moleküller birbirine daha yakın hale gelir ve gaz sıkışır. Bu duyarlılık, gazların fiziksel hallerini ve davranışlarını anlamamızda önemli bir rol oynar.
Umarım bu açıklamalar sorularınıza yeterince cevap olabilmiştir.
Selamlar,