
Nitrojen Gazı Özellikleri ve Faydaları Nelerdir?
Nitrojen gazı, atmosferimizin büyük bir kısmını oluşturan renksiz ve kokusuz bir bileşendir. Bu makalede, nitrojenin fiziksel ve kimyasal özellikleri, doğal kaynakları, endüstriyel kullanımları, tarımda ve sağlık üzerindeki etkileri detaylı bir şekilde ele alınmaktadır.
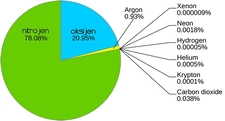
Nitrojen gazı (N₂), atmosferimizin yaklaşık %78'ini oluşturan renksiz, kokusuz ve tatsız bir gazdır. Kimyasal olarak, iki nitrojen atomunun güçlü bir üçlü bağ ile bir araya gelmesi sonucu oluşur. Nitrojen, çeşitli endüstriyel ve doğal süreçlerde önemli bir rol oynar. Bu makalede, nitrojen gazının temel özellikleri ve çeşitli faydaları üzerinde durulacaktır. Nitrojen Gazının Fiziksel ve Kimyasal Özellikleri Nitrojen gazı, birçok fiziksel ve kimyasal özelliğe sahiptir:
Nitrojen Gazının Doğal Kaynakları Nitrojen gazı, doğada bol miktarda bulunan bir elementtir. Doğal kaynakları arasında:
Nitrojen Gazının Endüstriyel Kullanımları Nitrojen gazı, çeşitli endüstriyel alanlarda yaygın olarak kullanılmaktadır:
Nitrojen Gazının Tarımdaki Rolü Tarımda nitrojen gazının önemli bir rolü vardır:
Nitrojen Gazının Sağlık Üzerindeki Etkileri Nitrojen gazı, insanlar için genellikle zararsızdır, ancak bazı durumlarda dikkatli olunmalıdır:
Sonuç Nitrojen gazı, birçok endüstride ve doğal süreçte önemli bir bileşendir. Fiziksel ve kimyasal özellikleri, tarımda, gıda endüstrisinde ve çeşitli teknolojik uygulamalarda yararlı olmasını sağlar. Ancak, nitrojen gazının doğru bir şekilde kullanılması ve yönetilmesi önemlidir; zira yüksek konsantrasyonları oksijen eksikliğine yol açabilir. Bu nedenle, nitrojen gazının faydalarını ve risklerini anlamak, hem endüstriyel hem de tarımsal uygulamalarda büyük önem taşır. |







































Nitrojen gazının bu kadar yaygın ve çok yönlü kullanım alanlarına sahip olması beni şaşırttı. Peki, bitkilerin nitrojen gazını doğrudan soluyamadıklarını öğrenmek beni düşündürdü. Bu durumda, bitkilerin nitrojen ihtiyacını karşılamak için hangi spesifik gübreler daha etkili olur? Ayrıca, nitrojen gazının tarımdaki kullanımıyla ilgili başka hangi önemli bilgiler var?
Merhaba Şezre,
Bitkilerin nitrojen ihtiyacını karşılamak için en yaygın ve etkili gübreler şunlardır:
1. Amonyum Nitrat: Bu gübre, bitkiler için hızlı ve etkili bir nitrojen kaynağı sağlar. Hem amonyum hem de nitrat şeklinde nitrojen içerir, bu da bitkilerin nitrojeni kolayca emmesine yardımcı olur.
2. Üre: Üre, en yaygın kullanılan nitrojen gübrelerinden biridir ve yüksek bir nitrojen içeriğine sahiptir. Toprakta mikroorganizmalar tarafından amonyum ve nitrat şekline dönüştürülerek bitkiler tarafından kullanılabilir hale gelir.
3. Amonyum Sülfat: Bu gübre, nitrojenin yanı sıra kükürt de içerir, bu da bitkilerin besin ihtiyacını daha kapsamli bir şekilde karşılar.
Nitrojen gazının tarımdaki kullanımıyla ilgili başka önemli bilgiler ise şunlardır:
1. Azot Sabitleyici Bakteriler: Bazı bitkiler, azot sabitleyici bakterilerle simbiyotik bir ilişki kurarak atmosferik nitrojeni kullanabilirler. Bu bakteriler, nitrojen gazını bitkilerin kullanabileceği bir şekle dönüştürür.
2. Toprak Verimliliği: Nitrojen, bitkilerin büyüme ve gelişmesi için kritik öneme sahiptir. Nitrojen eksikliği, bitkilerin soluk yeşil renkte olmasına ve büyüme geriliğine neden olabilir.
Umarım bu bilgiler sorularına cevap verir Şezre. Tarımla ilgili başka soruların olursa yardımcı olmaktan mutluluk duyarım!